- 製造業者は、自分自身とその製品を登録し、ヨーロッパ全体のEudamedデータベースを通じてデータを提出する必要があります。
-Each Medical Deviceは、製品のユニークな識別とトレーサビリティを実現することを目的として、製品とすべての高レベルのパッケージに適用する必要がある一意の識別番号(UDI)を搭載する必要があります。
EN 868
EN 868標準は、医療機器の滅菌包装専用であり、パッケージングが滅菌プロセス中にデバイスの無菌性を損なうことを保証します。
材料の安全性と互換性
包装材料が、さまざまな滅菌方法(蒸気滅菌、エチレンオキシドなど)を効果的にサポートし、デバイスの不妊を維持できるようにします。
一貫性と信頼性
汚染を防ぐために、滅菌後に包装が体力と完全性を維持していることを確認してください。
en iso 11607
医療機器用の滅菌された包装システムのEN ISO 11607標準は、滅菌バリアシステムのコア認証標準です。
世界的に信頼された品質
パッケージングは、滅菌、輸送、保管、使用のライフサイクル全体にわたって不妊の障壁を提供することを保証します。
包括的なテストと検証
この標準に準拠した製品は、ヒートシールの強度や漏れ検出などの厳密な物理的テストに合格し、その性能が医療機器包装の高い需要を満たすことを保証します。
en iso 11140
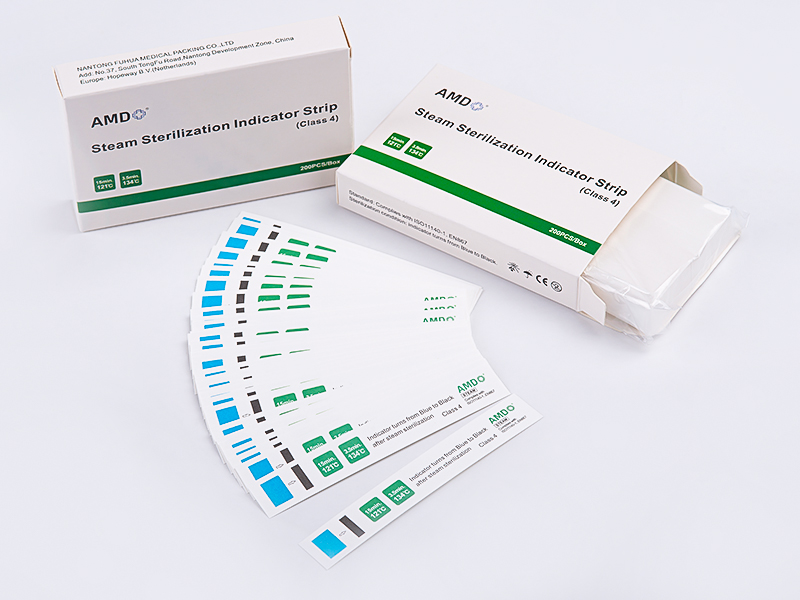
EN ISO 11140標準は、滅菌プロセスの有効性をテストするのに役立つ滅菌指標に焦点を当てています。
滅菌有効性の検証:インジケーターが使用された指標が、滅菌器具の使用を回避して、滅菌が正常に実行されたかどうかを明確かつ正確に示すことを保証します。
複数の滅菌方法の適用可能性:蒸気、エチレンオキシド、放射、その他の滅菌方法に適して、幅広いアプリケーションシナリオを確保します。













 「s-gravenweg 542、3065sgロッテルダムThe Netherlands
「s-gravenweg 542、3065sgロッテルダムThe Netherlands
 +31(0)10 254 28 08
+31(0)10 254 28 08







